전해가공 전해액의 최대 사용 수명 분석을 통한 폐기물 저감 연구
Abstract
This study aims to analyze the maximum service life of electrolytes used in Electrochemical Machining (ECM) to minimize chemical waste. In ECM processes, electrolytes are often discarded prematurely due to the absence of clear guidelines, resulting in increased waste and operational costs. To address this issue, a monitoring system equipped with pH, turbidity, temperature, and conductivity sensors was developed to measure electrolyte conditions in real time. The collected data was analyzed to determine the point at which the electrolyte can no longer be effectively used without compromising machining quality. The findings provide valuable insights into extending the electrolyte’s usage period, thereby reducing waste and enhancing the sustainability of ECM operations. This research contributes to improving resource efficiency and promoting environmentally friendly manufacturing practices.
Keywords:
Electrochemical machining (ECM), Electrolyte service life, Waste reduction, Electrolyte monitoring, Sustainable manufacturing1. 서 론
전해가공(electrochemical machining, ECM)은 복잡한 형상의 정밀 가공을 요구하는 다양한 산업 분야에서 핵심이다. ECM은 전기화학적 반응을 이용하여 금속을 용해시키는 가공 방식으로, 열 변형이나 기계적 충격을 최소화할 수 있어 높은 정밀도와 생산성을 제공한다. 그러나 ECM에서 사용되는 전해액(electrolyte)은 일정 기간 사용 후 폐기되어야 하며, 이 과정에서 상당한 양의 화학 폐기물이 발생한다. 기존의 ECM에서는 전해액의 교체 주기에 대한 명확한 기준이 부재하여 불필요한 조기 교체가 이루어지고 있으며, 이는 환경적 문제와 경제적 부담을 초래한다.
화학 폐기물은 재활용, 매립, 소각 등의 방법으로 처리되지만, 처리 과정에서 환경 오염을 초래한다. 매립 시 유해 물질이 토양과 지하수로 스며들어 환경 오염을 일으키며, 소각 시 대기 중으로 유독 가스가 방출되기도 한다. 또한, 폐기물 처리 비용이 부담되어 불법 투기나 비위생적인 매립이 발생하는 사례도 보고되고 있다. 경제적으로도 기업에 부담을 준다. 폐기물 처리비용은 기업 운영비용의 일부를 차지하며, 특히 중소기업은 재정적 부담이 될 수 있다. 국제무역연구원의 환경 규제 합리화 방안 연구에 따르면, 특정 화학물질을 등록하는데 최소 3억 원의 비용이 소요되며, 2008년부터 10년 동안 도입된 환경 규제는 총 509건으로 매년 평균 46건의 규제가 추가되고 있다. 이러한 규제의 시행 기간이 짧아 기업들은 대응을 하지 못하고 허가 취소나 폐쇄 명령을 받기도 한다. ECM 기업들도 전해액 폐기 규제로 인해 경제적 부담이 가중된다.
본 연구는 ECM에서 전해액의 최대 사용 수명을 분석해서, 가공 품질을 유지하면서도 전해액의 불필요한 교체를 방지하고 화학 폐기물을 저감하는 데 있다. 이를 위해 pH, Turbidity, Temperature, Conductivity의 특성을 실시간으로 모니터링할 수 있는 시스템을 개발하고, 실험적 데이터를 바탕으로 전해액의 수명 한계를 규명했다. 특히, 전해액이 어떻게 변화하는지를 분석하고, 전해액의 교체 시점을 결정하는 핵심 변수들을 도출하여, 전해액의 최대 활용 방안을 제시하고자 한다. 이러한 접근 방식을 통해 ECM 공정의 자원 효율성을 향상시키고, 산업 현장에서 지속 가능한 제조 공정을 할 수 있다[1-4].
2. 본 론
2.1 전해 가공(electrochemical machining, ECM)
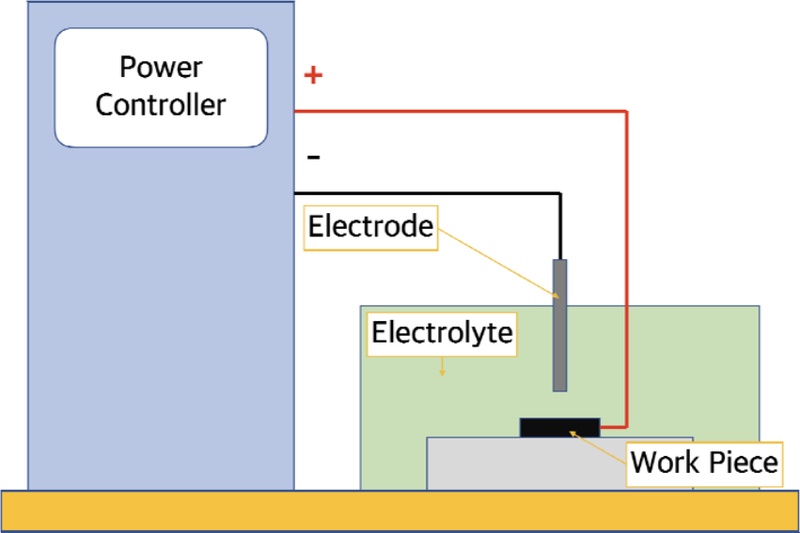
Fig. 1은 ECM의 개략도다. ECM은 금속의 표면을 전기화학적 방식으로 제거하는 가공 기술로, 비접촉 방식의 특성을 통해 복잡한 형상을 높은 정밀도로 가공할 수 있다. ECM은 전극과 가공물 사이에 ECM 전해액을 통해 전류를 공급함으로써 금속 이온을 용해시키는 원리다. ECM은 가공물에 열적 손상이나 기계적 변형을 최소화하며, 공구 마모가 발생하지 않는다는 점에서 효율적인 가공 공정으로 평가받는다.
2.2 전해액
ECM은 전해액을 매개로 가공물(workpiece)을 양극(anode)으로, 전극(electrode)을 음극(cathode)으로 설정하여 전류를 흘림으로써 가공물 표면에서 전기화학적 용해를 유도하는 것이다. NaCl은 ECM에서 가장 널리 사용되는 전해액 중 하나로, 물에 용해되었을 때 높은 전기 전도도를 제공하고, 다양한 금속의 가공에 적합한 특성을 보인다.
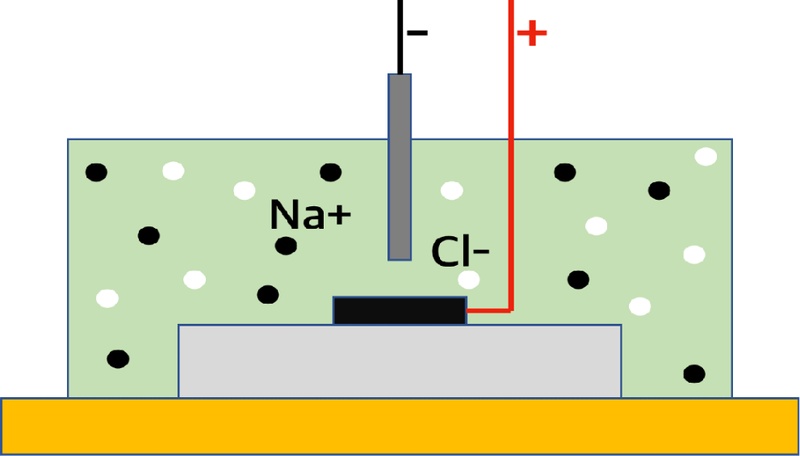
Fig. 2는 NaCl ECM process로 ECM 전해액은 Cl- 이온이 금속 표면에서 산화층 제거를 촉진하여 재료를 균일하게 제거할 수 있도록 한다. 본 연구는 ECM 전해액의 공정 중 변화하는 데이터(pH, turbidity, temperature, conductivity)를 실시간으로 측정하여 공정 중 최대의 전해액 교체 주기를 제안함으로써 화학 폐기물 감소를 위한 방법을 제시했다[5,6].
3. 시스템 구성
3.1 시스템 개요
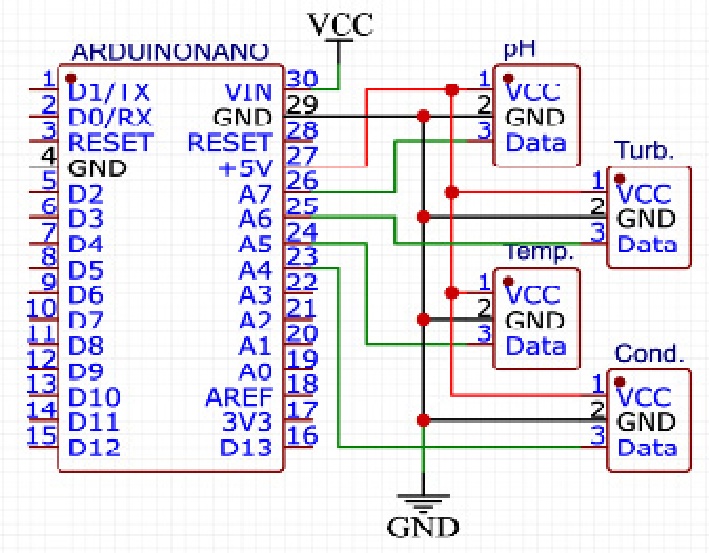
Fig. 3은 ECM 전해액을 통해 데이터를 측정할 수 있는 본 연구를 위한 장치로 ATmega328을 MCU (MicroController unit)로 사용하는 오픈소스 하드웨어 기반의 임베디드 시스템 중 하나인 Arduino Nano를 중심으로 4개의 센서(pH, turbidity, temperature, conductivity)를 통해 각각의 데이터를 실시간으로 측정할 수 있도록 했다[7-8].
3.2 측정 도구
시스템의 MCU가 Input Voltage 7~12 V, Operating Voltage 5 V, DC Current per I/O Pins20 mA(I/O Pins)인 Arduino Nano의 Specifications와 ECM 전해액의 온도가 0-60℃ 내외인 점을 고려해서 비교적 저렴하게 사용할 수 있는 측정 도구들을 선별했다[7,8].
pH sensor(Fig. 4)는 전해질의 산도를 측정하며, 이는 ECM의 효율성과 품질에 직접적으로 영향을 미칠 수 있다. 전해질의 pH가 적정 범위를 벗어나면 전기화학 반응의 속도가 변화하여 금속 제거 속도가 감소하거나, 공정 중 재료 및 장비의 부식 문제가 발생할 수 있다. pH sensor specifications(Table 1)는 Measuring range 0.0~14.0 pH, Accuracy ±0.1 pH(25℃), Measuring temperature 0~60℃이다. 정확도는 표준 완충 용액(4.01, 7.00, 10.01 pH)을 이용했다. 측정 전 완충 용액을 통해 교정된 기준값과 비교해서 편차를 확인하고, 보정 과정에서 발생할 수 있는 오차를 줄이기 위해 3회 반복 측정했다. 이를 통해 ±0.1 pH의 정확도를 유지하는지 확인했고, 측정값이 일정 기준을 벗어나면 보정했다.
Turbidity sensor(Fig. 5)는 전해질 내에 포함된 부유 입자의 농도를 측정하는데 사용된다. ECM 공정 중 전극과 금속 표면 사이에서 제거된 재료 입자가 전해질에 혼합되면서 전해질의 탁도가 증가한다. 이러한 탁도의 증가는 전해질의 전기적 성질을 저하시켜 공정의 효율성을 떨어뜨릴 수 있다. Turbidity sensor specifications (Table 2)는 Insulation resistance 100 M(Min), Measuring temperature 5~90℃이다. 정확도는 표준 탁도 용액(Formazin 표준 용액, 20, 100, 500 NTU)을 이용했다. 표준 용액을 통해 측정값을 비교하고, 보정 곡선을 작성해서 측정값의 정확성을 확보했다. 또한, 측정 시 주변 광원의 영향을 최소화하기 위해 동일한 환경에서 측정했으며, 반복성을 검증하기 위해 5회 반복 측정했다.
Temperature sensor(Fig. 6)는 ECM 중 전해질 및 공정 환경의 온도 변화를 모니터링한다. ECM 공정에서는 고전류가 흐르면서 열이 발생하고, 이는 전해질의 화학적 성질과 공정 효율성에 영향을 미친다. 전해질의 온도가 과도하게 상승하면 가공 정밀도가 저하될 뿐 아니라 전극과 금속 간의 반응에 변화를 초래할 수 있다. Turbidity sensor specifications(Table 3)는 Insulation resistance 100 M(min), Measuring temperature 5~90℃이다. 정확도는 NIST(national institute of standards and technology) 인증된 기준 온도계와 비교 측정했다. 기준 온도계와 동일한 조건에서 측정 후, 평균 오차를 계산해서 보정 계수를 도출했다. 또한, 온도 변화에 따른 반응 속도를 검증하기 위해 센서를 10℃, 25℃, 50℃, 75℃의 온도 환경에서 측정 후, 기준 온도계와의 편차를 분석했다.
Conductivity sensor(Fig. 7)는 전해질의 전기 전도도를 측정한다. 전도도는 전해질 내 이온 농도를 반영하며, 전도도가 높을수록 전류 흐름이 원활해지고 가공 속도가 증가한다. 그러나 전도도가 과도하게 높으면 단락 현상이 발생할 수 있으며, 반대로 전도도가 낮으면 전기화학 반응이 충분히 발생하지 않아 공정이 비효율적으로 진행될 수 있다. Conductivity sensor specifications(Table 4)는 Measuring range 0~1000 ppm, Accuracy ±10% F.S.이다. 정확도는 KCl(염화칼륨) 표준 용액(84 µS/cm, 1413 µS/cm, 12.88 mS/cm)을 사용했다. 각 표준 용액에서의 측정값을 기준값과 비교해서 오차를 확인하고, 이를 기반으로 보정 계수를 설정했다. 또한, 센서의 반복 측정 신뢰성을 확보하기 위해 동일한 용액에서 3회 반복 측정했다.
4. 실험 조건
4.1 시스템 구축
Table 5는 pH sensor를 통해 ECM 전해액의 pH 데이터를 측정하기 위한 시스템이다. pH sensor는 화학 반응 특성에 의해 출력값이 비교적 천천히 변화하기에 10 ms~50 ms의 주기 맞추고, 특히 30 ms는 데이터가 비교적 안정화된 상태에서 샘플링하기 적절한 주기이다. 만일 너무 짧으면 노이즈가 포함될 수 있고, 너무 길면 실시간 데이터 확보가 어렵다. 이를 통해 데이터는 30 ms 주기로 읽어 버퍼에 저장한 뒤, 중간값 필터링을 적용하여 노이즈를 감소시켰다.
Table 6은 Turbidity sensor를 통해 ECM 전해액의 탁도 데이터를 측정하기 위한 시스템이다. Turbidity sensor는 사용되는 MCU의 전압을 기반으로 탁도를 계산하기에 5.0/1023.0을 하게 되었는데, 이는 사용되는 MCU의 기본 전원 공급 전압이 5 V이기에, Turbidity sensor의 출력 전압도 5 V 내에서 정해지고, 이는 ADC 값을 전압으로 변환할 때 기준 전압으로 5.0 V를 사용함을 의미한다. 이때, 사용되는 MCU의 ADC는 10비트 해상도를 가지기에 입력 전압이 0~1023의 범위를 가진다.
Table 7은 Temperature sensor를 통해 ECM 전해액의 온도 데이터를 측정하기 위한 시스템이다. Temperature sensor는 저항기의 일종인 Thermistor를 사용했기에 저항값 계산을 해야 하고, 이는 전압 분배 회로를 기반으로 이루어진다. 저항값은 스테판-볼츠만 방정식에 의해 온도로 변환되며, 보정 계수를 통해 정확성을 유지한다. 1023은 사용되는 MCU의 ADC는 10비트 해상도를 가지기에 해상도에 맞춰 데이터를 변환하는 것을 알 수 있고, 전압 분배 회로에서 기준 저항으로 사용되는 값인 SERIES_RESISTOR는 일반적으로 10 kΩ의 고정 저항이 사용되기에 이는 Thermistor의 온도 특성과 함께 최적의 분배 전압 범위를 설정하기 위함이다. 마지막으로 -273.15는 계산된 온도의 단위가 켈빈(K)이기에 이를 ℃로 변환하기 위해 사용했다.
Table 8은 Conductivity sensor를 통해 ECM 전해액의 전기전도도 데이터를 측정하기 위한 시스템이다. Conductivity sensor는 온도 변화에 따라 변화를 보정하기에 온도 보정계수를 사용한다. 이때 사용된 온도 보정계수는 일반적으로 물의 Conductivity가 측정되는 25.0℃를 기준으로 25.0을 기입했다. 온도 변화에 따라 변화하는 전기전도도의 변화는 온도 1℃ 증가에 따라 약 1.85% 증가하는 물의 전기전도도의 기준에 맞춰 이를 보정하기 위해 1.0+0.0185를 사용했다.
4.2 ECM 실험
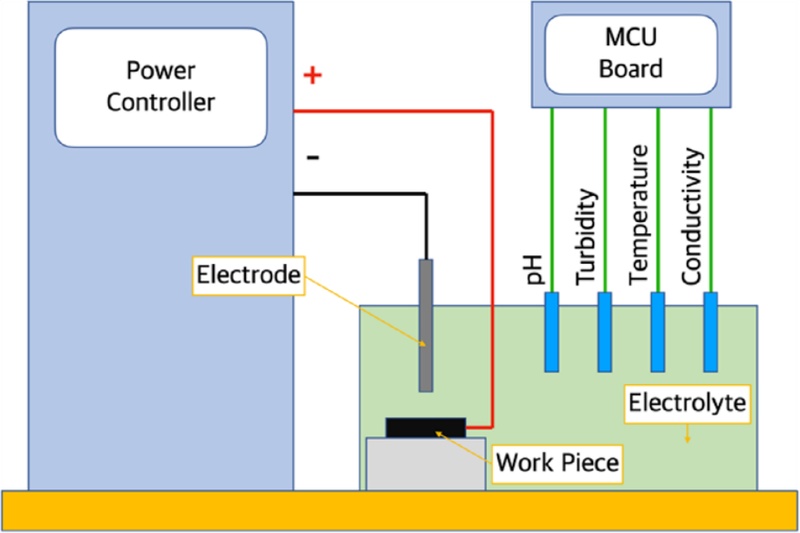
Fig. 8은 ECM 중 ECM 전해액의 공정 중 변화하는 데이터(pH, turbidity, temperature, conductivity)를 측정하는 방법이고, Fig. 9는 이를 위한 실험 환경이다. 실험은 ECM 전해액의 교체 없이 총 10회의 실험하는 도중의 데이터 뿐 아니라, 실험하기 전후의 데이터 또한 확보해서 경향을 분석하고자 했다. 실험 조건은 Table 9에 제시되어 있으며, 10 A의 일정한 전류가 적용되었다. 간극은 3 mm로 설정되었으며, 전극은 직경(Ø) 1.5 mm의 텅스텐 전극, Workpiece는 SUS304로 준비했다. 또한, 전해질로는 0.2 mol 농도의 NaCl이 사용되었고, 각 실험은 5 min씩 진행되었다. Power supplier는 총 2대를 사용했는데, 1대는 ECM, 다른 1대는 데이터 수집을 위한 것이다.
4.3 ECM의 ECM 전해액
Fig. 10(a)는 0.2 mol of NaCl에 Electrode와 Workpiece를 넣은 실험 전, Fig. 10(b)는 1회의 실험을 거친 실험 후에 대한 것이다. 1회의 실험을 했음에도 불구하고 색과 투명도에 큰 변화가 발생했음을 알 수 있고, 실제 데이터를 측정하며 색과 투명도 외에 다른 변화가 있는지 분석했다.
5. 실험 결과
5.1 Workpiece
Fig. 11(a)은 ECM에서 첫 번째 Workpiece의 결과로, Ø1.5 mm 텅스텐 전극을 사용하여 가공한 결과 중심부가 파였으며 전류가 약 8.7 mm 정도로 퍼진 것을 확인할 수 있다. 반면, Fig. 11(b)은 동일한 조건으로 가공한 일곱 번째 Workpiece의 결과로, 중심부의 파임 현상이 발생하지 않았으며 전류는 약 10.8 mm 정도로 퍼진 것을 보여준다. 이를 통해 동일 조건에서 ECM electrode를 반복적으로 사용하면, 일곱 번째 작업부터 ECM 전해액의 성능이 현저히 저하되어 더 이상 사용하기 어렵다는 점을 확인할 수 있었다. 따라서, 안정적이고 균일한 ECM를 유지하기 위해 ECM 전해액은 일곱 번째 작업 이후 교체해야 한다는 결론을 도출할 수 있다.
본 연구는 특정 조건에서 전해액의 교체 주기를 도출하는 것이 아니라, 다양한 가공 조건에서 적용 가능한 전해액 수명 평가 기준을 확립하는 것이다. 일곱 번째 작업에서 전해액의 성능 저하되었지만, 이는 특정 전류 밀도, 전극 크기, 전해액 조성 등의 조건에서 도출된 결과이며, 다른 공정 조건에서는 동일한 기준이 적용되지 않을 수 있다. 따라서, 5.2절부터는 sensor 데이터 분석(pH, turbidity, temperature, conductivity)을 통해 전해액 특성이 실험 횟수에 따라 어떻게 변화하는지 평가하고, 변수들이 전해액의 성능 저하와 어떤 상관관계를 가지는지를 규명하고자 한다.
5.2 측정 data
본 실험에서는 ECM 전해액의 공정 중 실시간으로 변화를 측정하고 분석했다. 측정된 데이터는 초기 상태(0), 최종 상태(10), Start data(0.5, 1, 1.5 등), 그리고 Stop data(1, 2, 3 등)으로 구분되며, 이를 통해 ECM이 진행됨에 따라 전해액의 특성이 어떻게 변화하는지 체계적으로 분석할 수 있도록 했다.
본 연구에서 초기 상태(0)는 ECM 공정을 수행하기 전 전해액의 상태를 의미하며, 최종 상태(10)는 ECM을 10회 수행한 후의 전해액 상태를 나타낸다. ECM이 진행되는 과정에서 전해액의 실시간 변화를 측정하기 위해 Start data(0.5, 1, 1.5 등)와 Stop data(1, 2, 3 등) 개념을 도입했다.
Start data는 ECM이 진행되는 중간 단계를 의미하며, ECM이 특정 시점(예: 0.5, 1, 1.5 등)까지 수행된 시점에서 측정된 데이터를 나타낸다. 반면, Stop data는 ECM이 특정 단계까지 완료된 후 전해액의 상태를 나타내는 값으로, ECM 반응 이후 측정된 결과를 의미한다. 예를 들어, ECM 0.5단계 수행 후 측정된 전해액의 값이 1이라면, 이는 Stop data로 기록되며, ECM이 1.5단계까지 진행된 후 측정된 값이 2라면 해당 값도 Stop data에 해당한다.
이를 통해 ECM 중 전해액의 변화 과정을 체계적으로 분석할 수 있으며, Start data와 Stop data를 비교함으로써 ECM 단계별 전해액의 전기화학적 특성 변화를 확인할 수 있다.
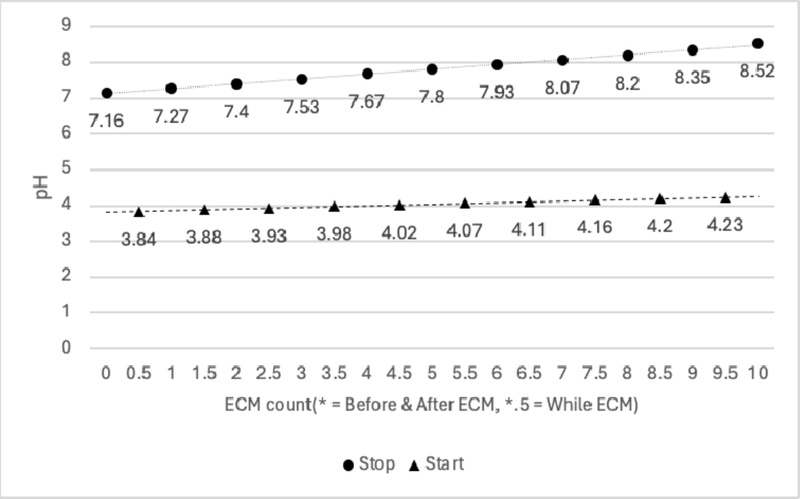
pH data(Fig. 12)는 7.16으로 중성에 가까운 값이었으나, 공정 초반에 급격히 3.84까지 낮아졌다. 이는 전극과 전해질 간 강력한 전기화학적 반응으로 수소 이온 농도가 증가했기 때문으로 해석된다. 이후 Start data는 3.84에서 4.23 범위를 유지하며 안정적인 경향을 보였고, Stop data는 7.16에서 8.52까지 점진적으로 상승하며 공정 후반부에 전해질 내 화학적 반응이 안정화되면서 알칼리성이 증가한 결과로 보인다. Start data는 일정한 범위를 유지했으나, Stop data는 시간이 지남에 따라 지속적으로 상승했다.
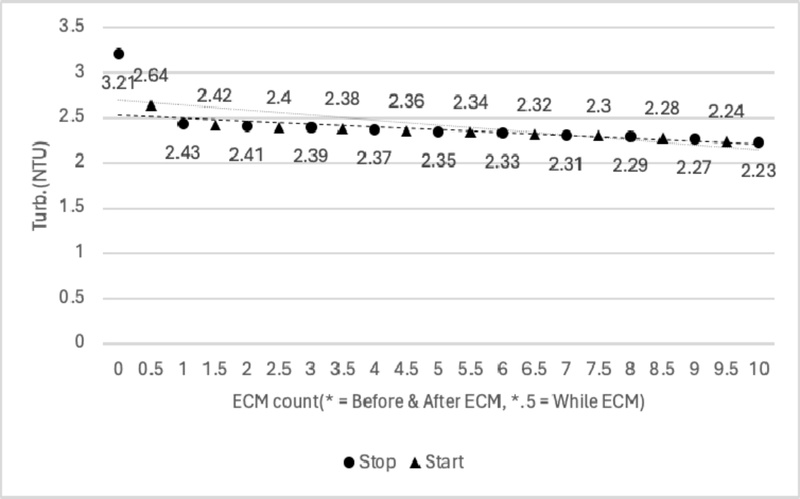
Turbidity data(Fig. 13)가 높을수록 ECM 전해질이 더욱 깨끗하고 공정 수행에 적합한 상태다. Turbidity는 3.21 NTU로, 높은 수준의 청결도를 보였다. 그러나 공정 초반에는 값이 급격히 낮아져 2.43 NTU를 기록했으며, 이는 ECM 과정에서 생성된 불순물이 전해질 내에 분산되어 투명도가 저하되었기 때문이다. Turbidity data의 감소는 전해질 내 불순물이나 부유물이 축적되어 전해질 상태가 점점 열악해지는 현상을 나타낸다. Start data와 Stop data는 모두 시간이 지남에 따라 꾸준히 감소하여 공정 종료 시점에는 가장 낮은 값을 기록했다.
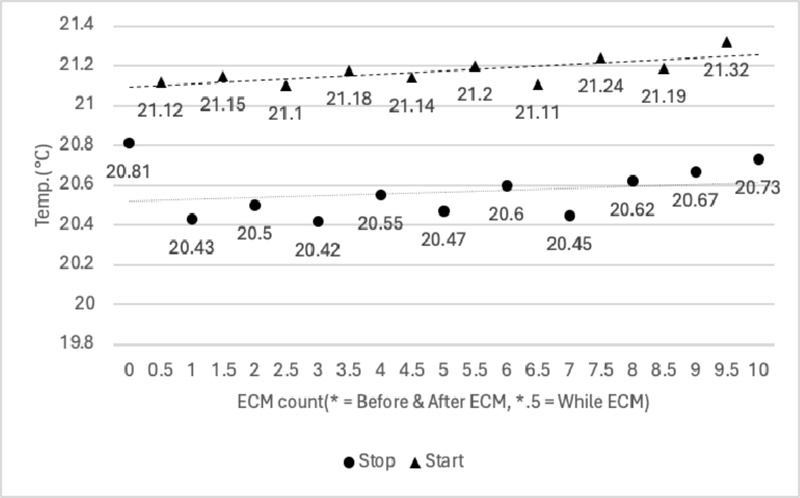
Temperature data(Fig. 14)는 초기에 20.81oC로 시작해서ECM 동안 20.43℃과 21.32℃ 사이에서 변동하는 모습을 보였다. 초반에는 약간의 온도 감소가 나타났으나, 이후 점차 상승하는 경향을 보이며, Start data는 최고 21.32℃에 도달했다. 반면 Stop data는 공정 진행 동안 20.43℃에서 20.73℃로 상승했다. 실험 종료 시점에서 Stop data는 20.73℃로 초기값과 유사한 수준으로 회복되었다. 이러한 온도의 변화는 ECM에서 전기화학적 반응으로 인해 발생하는 열 에너지와 전해질의 냉각 효과 간의 균형으로 설명될 수 있다.
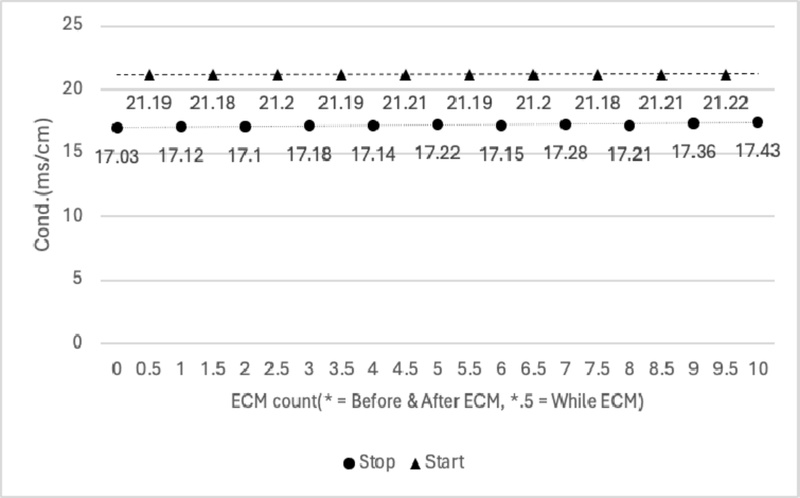
Conductivity data(Fig. 15)는 실험 초기 17.03 ms/cm에서 시작해서 ECM 중 최대 21.21 ms/cm까지 증가했고, 공정 종료 시점에는 17.43 ms/cm로 초기 값보다 소폭 증가한 수준의 data가 측정되었다. 초반에는 전극과 전해질 간의 전기화학적 반응으로 인해 이온 농도가 급격히 증가하며 전기전도도가 상승하였다. 이후 공정 중반부터는 생성된 이온들이 전해질 내에서 균일하게 분포하면서 전기전도도가 안정적인 범위를 유지했다. 최종적으로 전기전도도가 초기보다 증가한 것은 공정 중 생성된 이온의 잔존으로 해석된다.
6. 결 론
본 연구는 ECM 공정에서 전해액의 최대 사용 수명을 분석하여 화학 폐기물 저감을 위한 방안을 모색했다. ECM에서는 전해액의 교체 시점을 명확히 판단하지 못해 불필요한 자원 낭비와 운영 비용이 증가하는 문제가 발생한다. 이를 해결하기 위해 본 연구에서는 전해액 특성(pH, turbidity, temperature, conductivity)을 실시간으로 모니터링하는 시스템을 구축하고, 전해액의 성능 저하 시점을 분석했다.
먼저 실험을 통해 전해액의 성능 변화를 관찰하기 위해 전해액 데이터를 측정했고, 일곱 번째 Workpiece에서 가공 품질의 저하가 확인되었다. 이후 센서 데이터를 분석한 결과, 특정 패턴이 반복적으로 나타나는 것을 확인했다.
Workpiece의 가공 결과를 비교한 결과, 첫 번째 Workpiece에서는 중심부가 명확하게 가공되었으나(Fig. 11(a)), 일곱 번째 Workpiece에서는 가공 깊이가 감소하고 전류 분포가 넓어지는 현상이 나타났다(Fig. 11(b)). 이를 통해 특정 조건에서 전해액의 저하가 가공 품질 저하로 이어질 수 있음을 확인했다. 특정 데이터 패턴(pH, turbidity, temperature, conductivity)이 발생하면, Workpiece 가공 품질이 저하될 가능성이 높음을 확인했다. 따라서, 다른 실험 조건에서도 유사한 데이터 패턴이 나타나면, 유사한 문제가 발생할 가능성이 있음을 알 수 있다.
ECM이 진행되는 중간 단계를 의미하는 Start data를 기준으로 pH data는 초기 3.84에서 4.23까지 상승할 때 일곱 번째 데이터는 4.16(Fig. 8), Turbidity data는 2.64 NTU 에서 2.24 NTU까지 감소할 때 일곱 번째 데이터는 2.3 NTU (Fig. 9), Temperature data는 21.12℃에서 21.32℃까지 상승할 때 일곱 번째 데이터는 21.24℃(Fig. 10), Conductivity data는 21.19 ms/cm에서 21.22 ms/cm까지 상승할 때 일곱 번째 데이터는 21.18 ms/cm(Fig. 11)다. 이는 가공이 진행됨에 따라 전해액 내의 불순물이 축적되고, 전극과 전해질 간의 전기화학적 변화가 발생함을 의미한다.
본 연구에서는 특정 실험 조건에서 일곱 번째 Workpiece 이후 전해액의 교체가 필요하다는 결론을 도출했으나, 이는 보편적인 기준은 아니다. 개별 공정 환경과 실험 조건에 따라 전해액의 교체 주기는 달라질 수 있으며, 이를 정확히 규명하기 위해서는 각 실험 조건에 따라 반복적인 실험과 데이터 분석이 필요하다. 본 연구는 전해액의 성능 저하와 가공 품질 저하 간의 상관관계를 제시함으로써, 향후 ECM 공정에서 객관적인 전해액 교체 기준을 마련하는데 기여할 수 있다.
References
- Kim, J. Y., Choi, S. G., Lee, E. S., 2019, Analysis of Machining Shape and Characteristics through Electro Chemical Fusion Process, Proc. Korean Soc. Manuf. Technol. Eng. Spring Conf., 47.
- Jeon, D. H., Kim, B. H., Chu, C. N., 2006, Micro Machining by EDM and ECM, Journal of the Korean Society for Precision Engineering, 23:10 52-59.
-
Gong, W., Dong, H., Zhou, J., Qiu, Y., Chen, C., You, P., 2022, Research Progress of Electrical Discharge and Electrochemical Hybrid Machining Technology, Proceedings of the 2022 5th World Conference on Mechanical Engineering and Intelligent Manufacturing (WCMEIM), 269-275.
[https://doi.org/10.1109/WCMEIM56910.2022.10021416]
-
Tang, L., Feng, X., Huang, T. Q., Liu, J., Zhang, J. J., Lei, Q. B., Wang, Z., 2019, Research on the Combined Electrochemical Machining and Electrical Discharge Machining Technology for Closed IntegerImpeller, Int. J. Adv. Manuf. Technol., 102 3419-3429.
[https://doi.org/10.1007/s00170-018-03231-7]
- Lee, E. S., Kim, C. K., 2003, A Study on Machining Characteristics of the Electropolishing of Aluminum Alloy, J. Korean Soc. Manuf. Technol. Eng., 12:2 17-22.
- Jang, S. H., Choi, S. G., Kim, S. H., Lee, E. S., 2022, A Study on the Improvement of Surface Roughness by Rotation of Workpieces through Dynamic Analysis of Electrochemical polishing, Proc. Korean Soc. Prec.ision Eng. Autumn Conf., 5.
-
Luan, X., Zhang, S., Li, G., 2018, Modified Power Prediction Model Based on Infinitesimal Cutting Force During Face Milling Process, Int. J. of Precis. Eng. and Manuf.-Green Tech., 5 71-80.
[https://doi.org/10.1007/s40684-018-0008-7]
- Choi, S. G., 2020, Study on Precision Electrochemical Machining Characteristics Based on Deep Learning, Doctorate Thesis, Inha University, Republic of Korea.

Ph. D. Candidate in the Department of Mechanical Engineering, Inha University. His research interest is System Analysis.
E-mail: 222191500@inha.edu

Ph. D. Student in the Department of Mechanical Engineering, Inha University. His research interest is Electro Chemistry.
E-mail: preferjang@inha.edu

Ph. D. in the KIURI Center for Hydrogen Based Next Generation Mechanical System, Inha University. His research interest is Mechanical Design.
E-mail: choisg@inha.ac.kr

Professor in the Department of Mechanical Engineering, Inha University. His research interest is Electrochemical Polishing.
E-mail: leees@inha.ac.kr